エーザイ:Biogen、AducanumabをFDAに申請へ:早期アルツハイマー症状悪化抑制(動画):
Biogen Filing for Aducanumab in Alzheimer’s Disease on New Analysis from Phase 3:
Biogen计划根据第三阶段研究的新分析,制定针对阿兹海默症的Aducanumab的监管备案
2019年10月22日
エーザイ/バイオジェン・インク
早期アルツハイマー病;治療薬
早期アルツハイマー病の臨床症状悪化を抑制(主要項目および副次項目)するため、大規模データセットで、新たな解析・評価を実施しました。
2020年の早い時期に新薬承認申請することで、米国食品医薬品局(FDA)と協議中。
治療薬: Aducanumab
これまでの臨床試験に登録された被験者のうち、適格な方に Aducanumabを提供します。
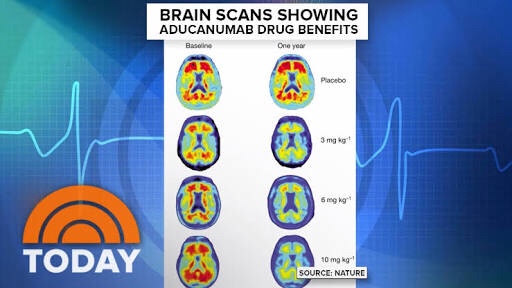
Aducanumab:解析・評価結果
大規模データセットでの、新たな解析・評価では、良好な結果を示しています。
これは、 Aducanumabの高用量投与が拡大したことによるものです。
ニュースリリース:2019年 | エーザイ株式会社
https://www.eisai.co.jp/news/2019/news201979.html
Biogen Plans Regulatory Filing for Aducanumab in Alzheimer’s Disease Based on New Analysis of Larger Dataset from Phase 3 Studies
October 22, 2019
Biogen Inc.
Eisai Co., Ltd.
New analysis of larger dataset showed that aducanumab reduced clinical decline in patients with early Alzheimer’s disease as measured by the pre-specified primary and secondary endpoints
Based on discussions with the FDA, the Company plans to submit a Biologics License Application in early 2020
Biogen aims to offer aducanumab to eligible patients previously enrolled in clinical studies
The positive results of this new analysis were driven primarily by greater exposure to high dose aducanumab in the larger dataset as compared to data available at the time of the futility analysis
News Release:2019 | Eisai Co., Ltd.