💊FDA PHARMA today
ロシュ(Roche) – FDA、早期乳癌のアジュバント(手術後)治療薬として、ロシュのPerjeta(パーツズマブ)を承認
米国食品医薬品局(FDA)は、HER2陽性早期のアジュバント(手術後)治療での、ハーセプチン(登録商標)(トラスツズマブ)およびPerjeta(パーツズマブ:化学療法・Perjetaベースのレジメン)との組合せ処方を承認しました。
https://www.roche.com/media/store/releases/med-cor-2017-12-21b.htm
Roche – European Commission approves Roche’s Alecensa (alectinib) as first-line treatment in ALK-positive lung cancer
https://www.roche.com/investors/updates/inv-update-2017-12-21.htm
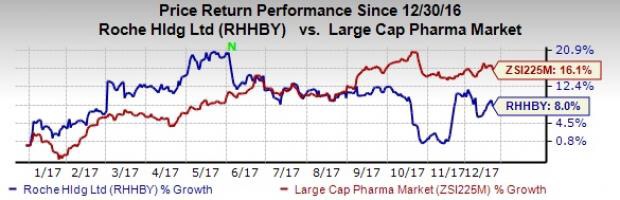
Roche’s Perjeta Gets FDA Nod for Post Surgery Breast Cancer – December 21, 2017 – Zacks.com
https://www.zacks.com/stock/news/286709/roches-perjeta-gets-fda-nod-for-post-surgery-breast-cancer
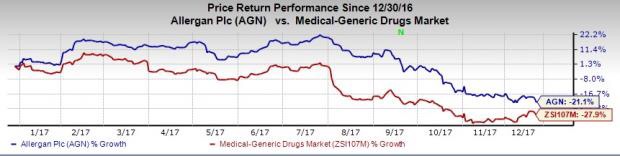
Allergan / Paratek、中等度・ 重症の尋常性ざ瘡で新薬申請(NDA)
Allergan plc AGNとパートナーParatek Pharmaceuticals PRTKは、9歳以上の患者を中等度〜 重症の尋常性ざ瘡対象に、1日1回の治験でSeysara(sarecycline)の新薬申請(NDA)を行いました。
FDAは2018年後半、結果回答の予定です。