
iPS cells:サルの膝軟骨を再製!
régénérer le cartilage du genou de singe !
Affen-Knieknorpel regenerieren!
regenerating monkey knee cartilage!
iPS細胞移植:再生猴膝軟骨!
ー4カ月後に組織が定着、免疫拒絶反応なしー
大阪大学:
「iPS細胞から作った軟骨組織を、サルの膝関節に移植すること」に成功した。
妻木範行教授(生化学):
2月20日、科学誌ネイチャーコミュニケーションズに発表した。
4カ月後に組織が定着、免疫による拒絶反応も確認されなかった。
iPS細胞の軟骨組織:
ーサルの膝関節に移植ー
- 軟骨は損傷すると、自然には修復しない。
- 新たな治療法開発につながることが期待される。
妻木教授らは、「膝関節軟骨が損傷した患者向けに、移植する臨床研究」を進めている。
研究チーム:
カニクイザルのiPS細胞から、「直径2~3ミリ程度の軟骨のかけら」を作製した。
サルの関節にかけらを移植:
軟骨が損傷した別のサルの関節に、複数のかけらを移植した。
すると、もともとあった周辺の軟骨と接着して、組織が再生した。
– 日本経済新聞
https://www.nikkei.com/article/DGXZQOUE206940Q3A220C2000000/
Greffe de cellules iPS : régénérer le cartilage du genou de singe !
-Tissu établi après 4 mois, pas de rejet immunitaire-
Université d’Osaka :
Ils ont réussi à “transplanter du tissu cartilagineux fabriqué à partir de cellules iPS dans les articulations du genou de singes”.
Professeur Noriyuki Tsumaki (Biochimie):
Le 20 février, il a été publié dans la revue scientifique Nature Communications.
Quatre mois plus tard, le tissu a été établi et aucun rejet immunitaire n’a été confirmé.
Cartilage des cellules iPS :
-Implanté dans l’articulation du genou d’un singe-
Lorsque le cartilage est endommagé, il ne se répare pas spontanément.
On s’attend à ce que cela conduise au développement de nouvelles méthodes de traitement.
Le professeur Tsumaki et ses collègues mènent “des recherches cliniques sur la transplantation chez les patients dont le cartilage de l’articulation du genou est endommagé”.
L’équipe de recherche:
Des « fragments de cartilage d’un diamètre d’environ 2 à 3 mm » ont été produits à partir de cellules iPS de singes cynomolgus.
Implantation de fragments dans des articulations de singe :
Des éclats ont été implantés dans l’articulation d’un autre singe avec du cartilage endommagé.
Ensuite, le tissu s’est régénéré en adhérant au cartilage environnant qui s’y trouvait à l’origine.
– Nihon Keizai Shimbun
Transplantation von iPS-Zellen: Affen-Knieknorpel regenerieren!
-Gewebebildung nach 4 Monaten, keine Immunabstoßung-
Universität Osaka:
Es gelang ihnen, „Knorpelgewebe aus iPS-Zellen in Kniegelenke von Affen zu transplantieren“.
Professor Noriyuki Tsumaki (Biochemie):
Am 20. Februar wurde es in der Fachzeitschrift Nature Communications veröffentlicht.
Vier Monate später wurde das Gewebe etabliert und es wurde keine Immunabstoßung bestätigt.
iPS-Zellknorpel:
-Ins Kniegelenk eines Affen implantiert-
Wenn Knorpel beschädigt ist, repariert er sich nicht spontan.
Es wird erwartet, dass dies zur Entwicklung neuer Behandlungsmethoden führen wird.
Professor Tsumaki und seine Kollegen führen “klinische Forschung zur Transplantation von Patienten mit geschädigtem Kniegelenkknorpel” durch.
Forschungsgruppe:
Aus iPS-Zellen von Cynomolgus-Affen wurden „Knorpelfragmente mit einem Durchmesser von etwa 2 bis 3 mm“ hergestellt.
Fragmente in Affengelenke implantieren:
Scherben wurden in das Gelenk eines anderen Affen mit beschädigtem Knorpel implantiert.
Dann regenerierte sich das Gewebe, indem es sich an den umgebenden Knorpel anheftete, der ursprünglich dort war.
– Nihon Keizai Shimbun
Engraftment of allogeneic iPS cell-derived cartilage organoid in a primate model of articular cartilage defect
Nature Communications
Abstract
Induced pluripotent stem cells (iPSCs) are a promising resource for allogeneic cartilage transplantation
to treat articular cartilage defects that do not heal spontaneously and often progress to debilitating conditions, such as osteoarthritis.
However, to the best of our knowledge, allogeneic cartilage transplantation into primate models
has never been assessed.
Here, we show that
allogeneic iPSC-derived cartilage organoids survive and integrate
as well as are remodeled as articular cartilage in a primate model of chondral defects in the knee joints.
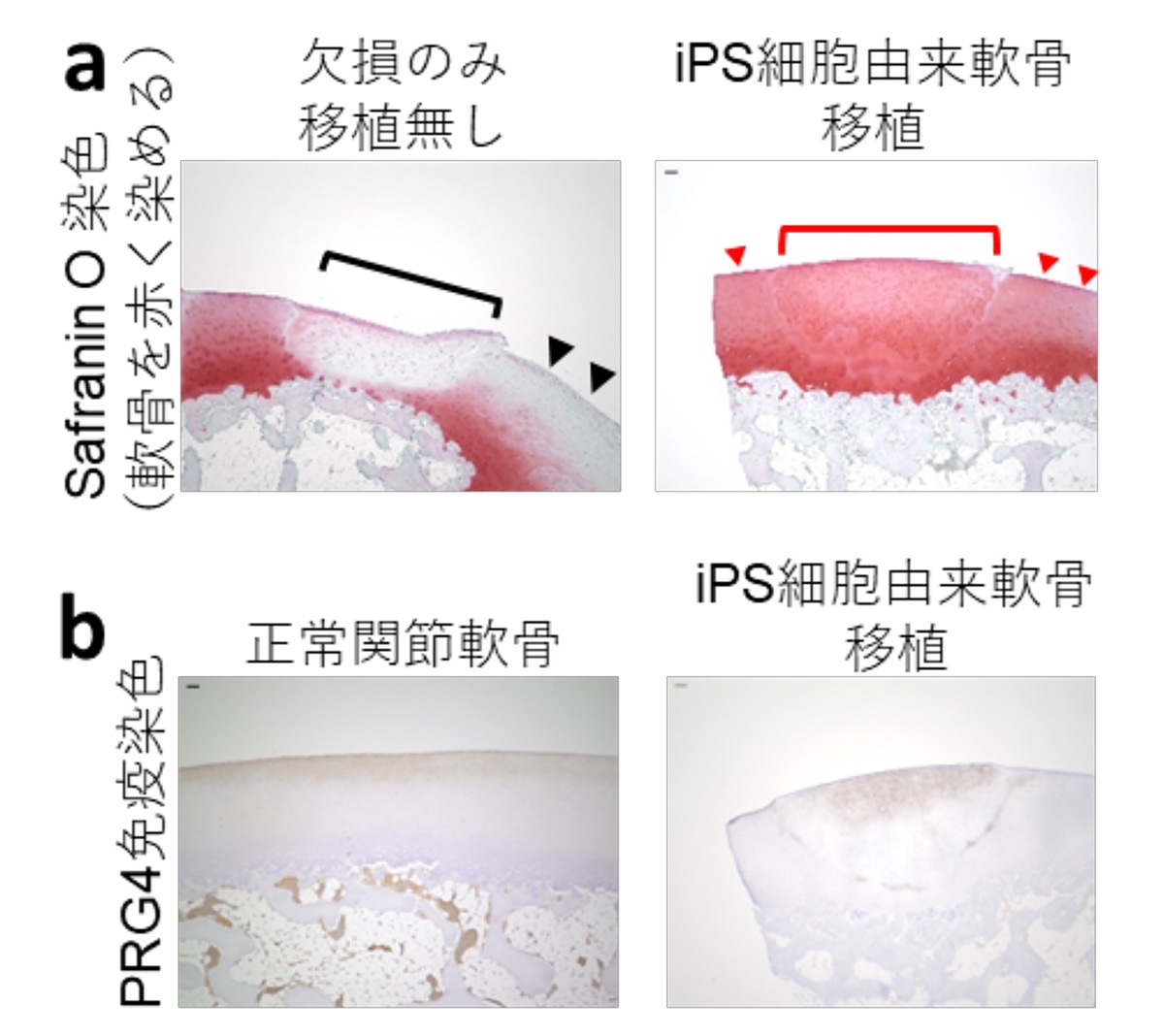
Histological analysis
revealed that allogeneic iPSC-derived cartilage organoids in chondral defects elicited no immune reaction and directly contributed to tissue repair for at least four months.
iPSC-derived cartilage organoids
integrated with the host native articular cartilage and prevented degeneration of the surrounding cartilage.
Single-cell RNA-sequence analysis indicated that
iPSC-derived cartilage organoids differentiated after transplantation, acquiring expression of PRG4 crucial for joint lubrication.
Pathway analysis suggested the involvement of SIK3 inactivation.
Our study outcomes suggest that allogeneic transplantation of iPSC-derived cartilage organoids
may be clinically applicable for the treatment of patients with chondral defects of the articular cartilage;
however further assessment of functional recovery long term after load bearing injuries is required.