京都大:iPSで成熟した心筋細胞作製に成功:トロポニン・タンパク質(動画):
Kyoto Univ: Pproduct of mature cardiomyocytes with iPS: Troponin protein:
京都大学:用 iPS 成功生产成熟心肌细胞:肌钙蛋白
ー京都大iPSグループ、創薬研究への応用期待ー
京都大iPS研究所
ヒトiPS細胞を用いて、新生児と同じ段階まで成熟した心筋細胞を作ることに成功した。
実際の心臓に近い細胞を再現できた。
再生医療や創薬研究への応用が期待される。
英科学誌ネイチャー・コミュニケーションズに6月21日掲載された。
iPS研究所:
吉田善紀准教授:心筋細胞の成熟度を示すトロポニンというタンパク質に着目。
iPS細胞から心筋細胞を作製する際にトロポニンを観測した。
約9千種類の化合物との反応を確認した。
ERRγ作動薬が効果:
その結果、ミトコンドリア機能の制御に関わる化合物ERRγ作動薬に注目。
「新生児並みに構造や代謝機能が成熟した心筋細胞を形成する効果のあること」が分かった。
また成熟に関わる遺伝子の発現も上昇していたという。
京都新聞
https://www.kyoto-np.co.jp/articles/-/585299
ヒトのiPS細胞から新生児レベルまで成熟した心筋細胞を作製する
ポイント
ヒトiPS細胞由来の心筋細胞はこれまで成熟度の低さが課題であった。
今回、化合物スクリーニング注1)により心筋細胞の成熟を促進する化合物(ERRγ作動薬注2))を同定した。
ERRγ作動薬で処理したヒトiPS細胞由来の心筋細胞は、T管構造注3)を有する。
構造的、代謝的、電気生理学的に新生児の心筋細胞に相当するレベルにまで成熟した。
本手法を用いることで、新生児レベルの心筋細胞を短期間で効率的に得られる。
今後の創薬研究や病態モデル、細胞治療などへの応用が期待できる。
CiRA | 京都大学 iPS細胞研究所
https://www.cira.kyoto-u.ac.jp/j/pressrelease/news/210621-180000.html
ERRγ enhances cardiac maturation with T-tubule formation in human iPSC-derived cardiomyocytes
Abstract
One of the earliest maturation steps in cardiomyocytes (CMs)
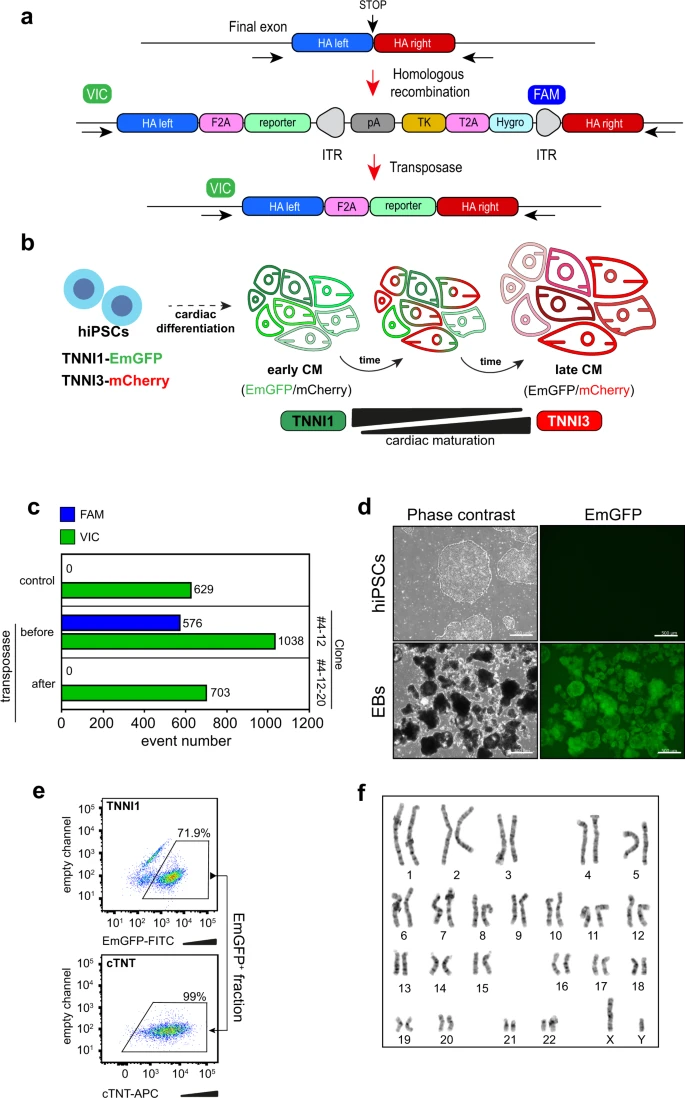
is the sarcomere protein isoform switch between TNNI1 and TNNI3 (fetal and neonatal/adult troponin I).
Here, we generate human induced pluripotent stem cells (hiPSCs)
carrying a TNNI1EmGFP and TNNI3mCherry double reporter to monitor and isolate mature sub-populations during cardiac differentiation.
Extensive drug screening
identifies two compounds, an estrogen-related receptor gamma (ERRγ) agonist and an S-phase kinase-associated protein 2 inhibitor, that enhances cardiac maturation and a significant change to TNNI3 expression.Expression, morphological, functional, and molecular analyses indicate that
hiPSC-CMs treated with the ERRγ agonist show a larger cell size, longer sarcomere length, the presence of transverse tubules, and enhanced metabolic function and contractile and electrical properties.
Here, we show that
ERRγ-treated hiPSC-CMs have a mature cellular property consistent with neonatal CMs and are useful for disease modeling and regenerative medicine.
Nature Communications