京都大学:利用 iPS 细胞进行癌症免疫治疗:增殖杀伤性 T 细胞
– 癌症免疫疗法的成本低于 1/10-
癌症免疫疗法:
攻击体内癌细胞的杀伤性T细胞,
从患者和捐赠者身上移植的“免疫疗法”
这是有效的。
然而,高成本一直是一个问题。
京都大学 iPS 细胞研究与应用中心
一群新教授金子
我们的目标是使用 iPS 细胞增殖 T 细胞。
然而,直到现在,“在增殖过程中对癌细胞的攻击”已经减少。
一种叫做 IL21 的物质:
因此,添加了一种叫做 IL21 的物质来增殖 T 细胞。
“有了 IL21,我们成功地保持了侵略性。”
T细胞的量产:
金子教授
如果 T 细胞的大规模生产成为可能,其成本将低于传统成本的十分之一。
他说他可以接受免疫治疗。
https://www.fnn.jp/articles/-/253309
生产“具有高增殖潜力的杀伤性T细胞克隆”
-有望应用于已采用的免疫疗法-
包起来:
在体外培养和激活免疫细胞并移植的治疗方法(过继免疫疗法)正在引起人们的关注。
然而,在刺激和增殖T细胞的过程中,细胞耗竭和衰老成为问题。
使用iPS细胞技术成功“克隆具有更高增殖能力的杀伤性T细胞”
过继免疫疗法:
它有望成为对抗癌症和艾滋病毒/艾滋病等慢性传染病的有力手段。
然而,
在产生大量T细胞的阶段,
由于细胞耗竭、老化和分化
挑战是降低增长能力。
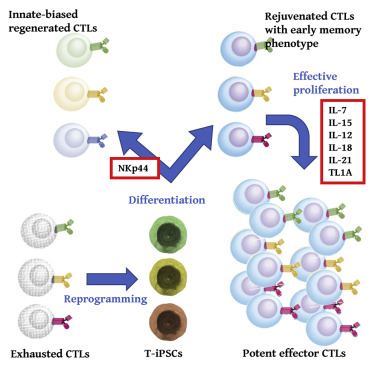
改良分化诱导法
因此,通过改进分化诱导方法,
具有很强的自我更新能力,
使用强大的效应 T 细胞,
我们创建了 iPSC-CTL,这是早期记忆 T 细胞的特征。
最佳条件下的增殖培养:
在优化条件下生长和培养时,iPSC-CTL 增殖超过 1015 倍。
使用该方法产生的 iPSC-CTL,
通过重新分化和扩展文化
无论是自体的还是异体的
预计“可以提供记忆T细胞和效应T细胞”。
本研究结果:
2021年10月6日发表在《分子疗法》上。
新闻|CiRA | 京都大学iPS细胞研究与应用中心
https://www.cira.kyoto-u.ac.jp/j/pressrelease/news/211013-160000.html
Generation of highly proliferative, rejuvenated cytotoxic T cell clones through pluripotency reprogramming for adoptive immunotherapy
Adoptive immunotherapy
has emerged as a powerful approach to cure cancer and chronic infections.
Currently, the generation of a massive number of T cells that provide long-lasting immunity
is challenged by exhaustion and differentiation-associated senescence, which inevitably arise during in vitro cloning and expansion.
To circumvent these problems,
several studies have proposed an induced pluripotent stem cell (iPSC)-mediated rejuvenation strategy to revitalize the exhausted/senescent T cell clones.
Because iPSC-derived cytotoxic T lymphocytes (iPSC-CTLs) generated via commonly
used monolayer systems have unfavorable, innate-like features such as aberrant natural killer (NK) activity and limited replication potential,
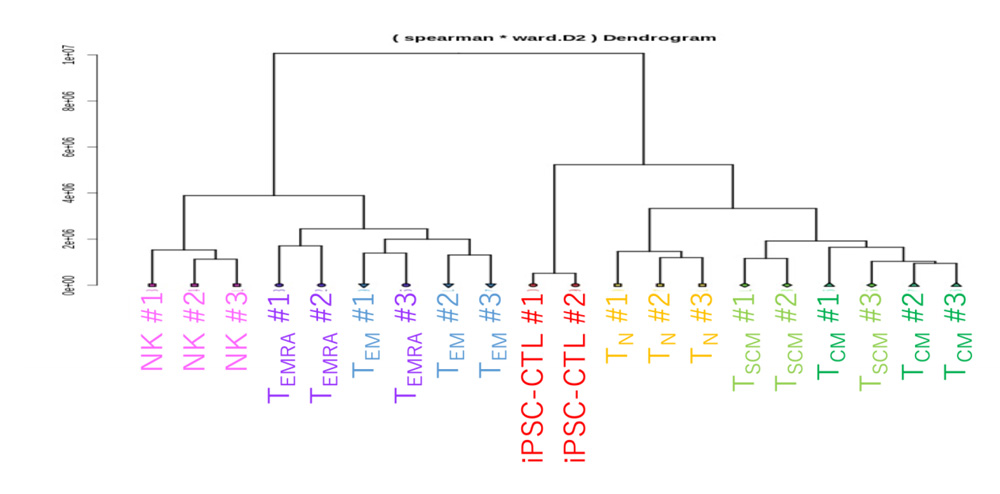
we modified the redifferentiation culture to generate CD8αβ+CD5+CCR7+CD45RA+CD56−-adaptive iPSC-CTLs.
The modified iPSC-CTLs
exhibited early memory phenotype, including high replicative capacity and the ability to give rise to potent effector cells.
In expansion culture with an optimized cytokine cocktail,
iPSC-CTLs proliferated more than 1015-fold in a feeder-free condition.
Our redifferentiation and expansion package of early memory iPSC-CTLs
could supply memory and effector T cells for both autologous and allogeneic immunotherapies.Molecular Therapy